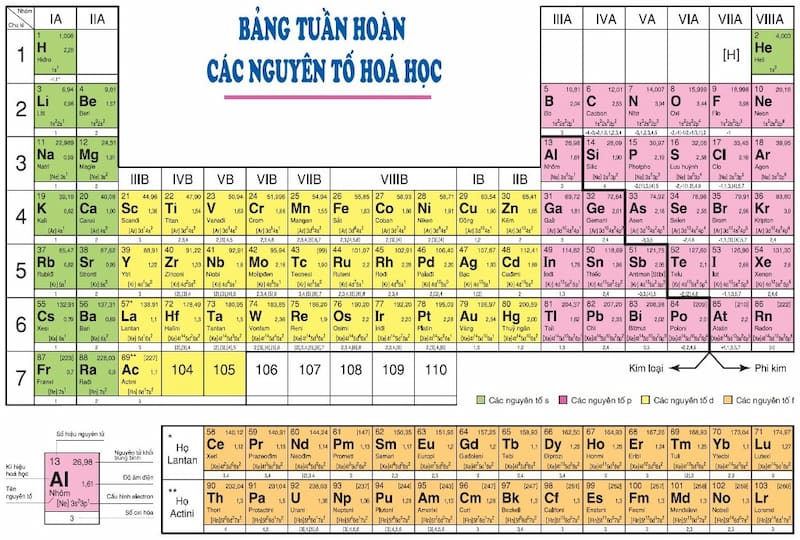
Hóa trị là một số biểu thị khả năng liên kết của nguyên tử nguyên tố với nguyên tử nguyên tố khác. Điều này được xác định dựa trên hóa trị của H là đơn vị và hóa trị của O là hai đơn vị. Có những nguyên tố chỉ có một hóa trị, nhưng cũng có những nguyên tố có nhiều hóa trị khác nhau.
Nội dung
- 1 Bảng hóa trị của các nguyên tố phổ biến nhất
- 2 Bảng hóa trị của một số nhóm nguyên tử phổ biến
- 3 Xác định hóa trị của một nguyên tố như thế nào?
- 4 Quy tắc hóa trị bạn cần nắm vững
- 5 Vận dụng quy tắc hóa trị để tính hóa trị và lập công thức hóa học
- 6 Những bài ca hóa trị giúp bạn ghi nhớ kiến thức dễ dàng
- 7 Bài tập thực hành vận dụng lý thuyết về hóa trị
Bảng hóa trị của các nguyên tố phổ biến nhất
Ghi nhớ hóa trị của các nguyên tố phổ biến sẽ giúp bạn tự tin hơn khi làm bài tập và không phụ thuộc quá nhiều vào công cụ tìm kiếm.
Dưới đây là bảng hóa trị của một số nguyên tố phổ biến:
Bảng hóa trị của một số nhóm nguyên tử phổ biến
Ngoài hóa trị của những nguyên tố hóa học phổ biến trên, bạn cũng nên ghi nhớ hóa trị của một số nhóm nguyên tử phổ biến.
Xác định hóa trị của một nguyên tố như thế nào?
Có 2 cách để xác định hóa trị của một nguyên tử. Đầu tiên, dựa vào khả năng liên kết của nguyên tử đó với hidro hoặc oxi:
- Nguyên tử nguyên tố khác liên kết được với bao nhiêu nguyên tử hidro, hóa trị của nguyên tố đó chính bằng số nguyên tử hidro đó. Hóa trị của H được coi là đơn vị.
Ví dụ, trong công thức hóa học của nước (H2O) thì oxi liên kết được với 2 nguyên tử hidro, vì vậy Oxi có hóa trị là II.
- Nguyên tử nguyên tố khác cũng được xác định bằng hai đơn vị dựa vào quy ước trên.
Ví dụ, với công thức hóa học của Canxi oxit (CaO) thì Ca có khả năng liên kết như O. Vì vậy, Ca có hóa trị là II.
Quy tắc hóa trị bạn cần nắm vững
Trước khi rút ra kết luận về quy tắc hóa trị, hãy thử đặt một phép tính đơn giản cho một công thức hóa học bất kỳ bao gồm hợp chất của hai nguyên tố (A, B), ký hiệu là AxBy. Trong đó, A có hóa trị là a và B có hóa trị là b. Chúng ta có thể dễ dàng nhận thấy tích của ax luôn bằng by.
Từ đây, ta có thể rút ra kết luận: Trong công thức hóa học, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia. Quy tắc này cũng đúng khi A và B là một nhóm nguyên tử.
Ví dụ, trong công thức hóa học của hợp chất Ca(OH)2: Ca có hóa trị là II, OH có hóa trị là I => 1 x II = I x 2.
Vận dụng quy tắc hóa trị để tính hóa trị và lập công thức hóa học
Biết hóa trị, chúng ta sẽ dễ dàng tính được hóa trị của một nguyên tố và lập công thức hóa học của hợp chất theo hóa trị.
Vận dụng 1: Tính hóa trị của một nguyên tố
Chúng ta có thể tham khảo ví dụ: Tính hóa trị của Sắt (Fe) trong hợp chất FeCl3 khi biết clo (Cl) có hóa trị bằng I.
Trả lời: Gọi hóa trị của Fe là a, ta có công thức 1 x a = 3 x I => a = III. Từ đây ta có thể kết luận Fe có hóa trị III.
Vận dụng 2: Lập công thức hóa học của hợp chất theo hóa trị
Cũng tương tự như tính hóa trị của một nguyên tố, khi biết hóa trị của các nguyên tố ta sẽ dễ dàng tìm được công thức hóa học của hợp chất.
Ví dụ, lập công thức hóa học của hợp chất được tạo bởi bạc hóa trị I và oxi.
Ta có công thức chung dạng: AgxOy. Theo công thức quy tắc hóa trị ta có: x x I = y x II => x/y = I/II = ½ => x = 1; y = 2. Công thức hóa học của hợp chất cần xác định là Ag2O.
Những bài ca hóa trị giúp bạn ghi nhớ kiến thức dễ dàng
Bài ca hóa trị (bài ca hóa học) là những bài ca dao, câu thơ có vần và nhịp điệu giúp các bạn học sinh ghi nhớ tên nguyên tố và hóa trị hóa học tương ứng dễ dàng.
Dưới đây là một vài bài ca hóa trị bạn có thể tham khảo:
Bài số 1:
Kali (K), Iot (I), Hidrô (H)
Natri (Na) với Bạc (Ag), Clo (Cl) một loài
Là hoá trị một (I) em ơi
Nhớ ghi cho kỹ kẻo thời phân vân
Magiê (Mg), Kẽm (Zn) với Thuỷ Ngân(Hg)
Oxi (O), Đồng (Cu), Thiếc(Sn) cùng gần Bari (Ba)
Cuối cùng thêm chú Canxi (Ca)
Hoá trị hai (II) nhớ có gì khó khăn
Bác Nhôm (Al) hoá trị ba (III) lần
In sâu trí nhớ khi cần có ngay
Cacbon (C), Silic (Si) này đây
Có hoá trị bốn(IV) không ngày nào quên
Sắt (Fe) kia lắm lúc hay phiền
Hai, ba lên xuống nhớ liền ngay thôi
Nitơ (N) rắc rối nhất đời
Một hai ba bốn, khi thời lên V
Lưu huỳnh (S) lắm lúc chơi khăm
Xuống hai lên sáu khi nằm thứ tư
Phot pho (P) nói đến không dư
Có ai hỏi đến thì ừ rằng năm
Em ơi, cố gắng học chăm
Bài ca hoá trị suốt năm cần dùng.
Bài số 2:
Hidro (H) cùng với liti (Li)
Natri (Na) cùng với kali (K) một loài
Ngoài ra còn bạc (Ag) ra oai
Nhưng hoá trị một đơn côi chẳng nhầm
Riêng đồng (Cu) cùng với thuỷ ngân (Hg)
Thường hai ít I chẳng phân vân gì
Đổi thay hai, bốn là chì (Pb)
Điển hình hoá trị của chì là hai
Bao giờ cùng hoá trị hai
Là ôxi (O), kẽm(Zn) chẳng sai chút gì
Ngoài ra còn có canxi (Ca)
Magiê (Mg) cùng với bari (Ba) một nhà
Bo (B) , nhôm (Al) thì hóa trị ba
Cácbon (C) silic (Si) thiếc (Sn) là bốn thôi
Thế nhưng phải nói thêm lời
Hóa trị hai vẫn là nơi đi về
Sắt (Fe) hai toan tính bộn bề
Không bền nên dễ biến liền sắt ba
Phốt Pho ba ít gặp mà
Photpho năm chính người ta gặp nhiều
Nitơ (N) rắc rối nhất đời
Một hai ba bốn, phần nhiều tới V
Lưu huỳnh lắm lúc chơi khăm
Khi hai lúc bốn, sáu tăng tột cùng
Clo Iot lung tung
Hai ba năm bảy nhưng thường một thôi
Mangan rắc rối nhất đời
Đổi từ một đến bảy thời mới yên
Hoá trị hai dùng rất nhiều
Hoá trị bảy cũng được yêu hay cần
Bài ca hoá trị thuộc lòng
Viết thông công thức đề phòng lãng quên
Học hành cố gắng cần chuyên
Siêng ôn chăm luyện tất nhiên nhớ nhiều
Bài tập thực hành vận dụng lý thuyết về hóa trị
Các bài tập thực hành về hóa trị sẽ giúp bạn củng cố lại kiến thức lý thuyết và vận dụng tìm hóa trị hay công thức hóa học của hợp chất.
Bài tập thực hành hóa trị 1
Hỏi: Hóa trị của một nguyên tố hay nhóm nguyên tố là gì? Và khi xác định hóa trị, lấy hóa trị của nguyên tố nào làm đơn vị, nguyên tố nào là hai đơn vị?
Trả lời: Hóa trị là con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác. Hóa trị của một nguyên tố được xác định theo hóa trị của H chọn làm đơn vị và hóa trị của O là hai đơn vị.
Bài tập thực hành hóa trị số 2
- Xác định hóa trị của mỗi nguyên tố có trong hợp chất sau: KH, H2S và CH4
- Xác định hóa trị của mỗi nguyên tố có trong hợp chất sau: Fe2O, SiO2
Trả lời:
- Ý số 1: Lấy hóa trị H là I làm đơn vị, ta dễ dàng xác định được: K hóa trị I; S có hóa trị là II; C có hóa trị là IV.
- Ý số 2: O có hóa trị là II, vì vậy Fe có hóa trị là I; Si có hóa trị là IV.
Bài học lý thuyết và công thức tính hóa trị rất đơn giản, chỉ cần lắng nghe thầy cô giảng bài trên lớp và chịu khó ôn luyện và làm bài tập về nhà các bạn học sinh sẽ dễ dàng nắm được kiến thức cơ bản. Hy vọng những kiến thức mà fptskillking.edu.vn tổng hợp trên đây sẽ giúp các bạn ôn tập bài học dễ dàng ngay tại nhà. Chúc các bạn học tốt!